Hisztamin
A Hisztamin világában végtelenül sok olyan szempont létezik, amelyek megérdemlik a gondos feltárást és elemzést. A Hisztamin eredetétől napjaink relevanciájáig lenyűgöző és vita tárgya volt. Ebben a cikkben egy utazásra indul a Hisztamin különböző aspektusain keresztül, a szociokulturális vonatkozásaitól a mindennapi életre gyakorolt hatásáig. Reflexió és mély elemzés révén felfedezheti a Hisztamin összetettségét és fontosságát a modern világban. Készüljön fel, hogy kitágítsa látókörét, és merüljön el a tudás és felfedezés univerzumában!

| |

| |
| Hisztamin | |
| IUPAC-név | |
| 2-(1H-imidazol-4-il)-etilamin | |
| Kémiai azonosítók | |
| PubChem | 774 |
| ChemSpider | 753 |
| EINECS-szám | 200-100-6 |
| DrugBank | DB05381 |
| KEGG | D08040 |
| ChEBI | 18295 |
| ATC kód | L03AX14 |
| InChIKey | NTYJJOPFIAHURM-UHFFFAOYSA-N |
| Beilstein | 2012 |
| Gmelin | 2968 |
| UNII | 820484N8I3 |
| ChEMBL | CHEMBL90 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | C5H9N3 |
| Moláris tömeg | 111,145 g/mol |
| Oldhatóság (vízben) | Jó |
A hisztamin (INN: histamine) egy nitrogén heterociklust tartalmazó amin. Neurotranszmitter, részt vesz a szervezet immunválaszának kialakításában, illetve a gyulladási folyamatokban. Receptorai: H1, H2, H3, H4.
A hisztamin szó a görög hisztosz (ιστός = szövet) és az ammónia összevonásából származik.[1]
Tulajdonságok
A hisztamin világossárga, higroszkópos kristályos anyag, amely olvadáspontja 84 °C. Vízben, metanolban, etanolban könnyen, éterben rosszul oldódik. Vizes oldatban tautomerizálódik: Nπ-H-hisztaminként és Nτ-H-hisztaminként fordul elő. Oldatban az utóbbi van többségben.
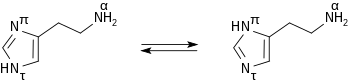
A molekula két bázikus nitrogénnel rendelkezik. Az egyik, az oldalláncon található alifás aminocsoport, a másik, az imidazol gyűrűn található két nitrogénatom közül az, amelyik nem rendelkezik hidrogénnel. Fiziológiás körülmények között az alifás nitrogén protonált (mivel a pKa értéke 9,4), míg az imidazol gyűrűn található nitrogén nem protonált (mivel a pKa értéke ≈ 5,8).
Előállítás és lebontás

A hisztamint a hisztidin dekarboxiláz enzim állítja elő hisztidinből, dekarboxilezéssel. A szervezet az előállított hisztamint tárolja, vagy inaktiválja lebontóenzimek segítségével, mint a hisztamin-N-metil-transzferáz(en) vagy diamino-oxidáz(en) (DAO).
Míg a központi idegrendszerben a szinapszisokba jutó hisztamint elsődlegesen a hisztamin-N-metil-transzferáz bontja le, addig a más szervekben található hisztamin metabolizmusát mindkét előbb említett enzim végzi. A hisztaminból keletkező metabolitokat további más enzimek alakítják tovább, melyek között szerepel a mono-amin-oxidáz-B(en) (MAO-B) és az aldehid-dehidrogenáz-2 (ALDH2(en)).
A baktériumok is képesek hisztamin előállítására hisztidin dekarboxiláz segítségével, ám ezek szerkezete eltér az állatokban található enzimekétől.
A hisztamin kis mennyiségben megtalálható a fermentációval előállított élelmiszerekben is, amelyet fermentációs baktériumok vagy élesztő állít elő. A borok 2–10 mg/l, a szaké 20–40 mg/l koncentrációban tartalmazhat hisztamint.
Jegyzetek
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 64. o. ISBN 963 8334 96 7
Fordítás
Ez a szócikk részben vagy egészben a Histamine című angol Wikipédia-szócikk fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Források
- Gyógyszerkémia I. (Tankönyvkiadó 1992) ISBN 963-184-356-4 (Szerkesztette: Tőke László, Szeghy Lajos)